近日,我院潘登余教授团队青年教师耿弼江在国际高水平期刊《Advanced Materials》(IF:29.4)上发表题为“Single Atom Catalysts Remodel Tumor Microenvironment for Augmented Sonodynamic Immunotherapy”的研究论文。

免疫治疗是一种通过激活机体先天和适应性免疫系统来抑制或杀伤肿瘤细胞的治疗策略,由于其卓越的疗效和创新性,免疫治疗曾在2013年被《科学》杂志评为年度最重要的科学突破。然而,目前的免疫治疗仍然存在一些局限性,如只有有限肿瘤类型能够有效应答,且会引发自身免疫并发症与其它脱靶毒性。研究证实,肿瘤免疫治疗的效果主要取决于复杂异质性的肿瘤微环境,由于“冷”肿瘤的低免疫原性和免疫抑制微环境,大多数实体瘤患者对免疫治疗几乎没有反应。
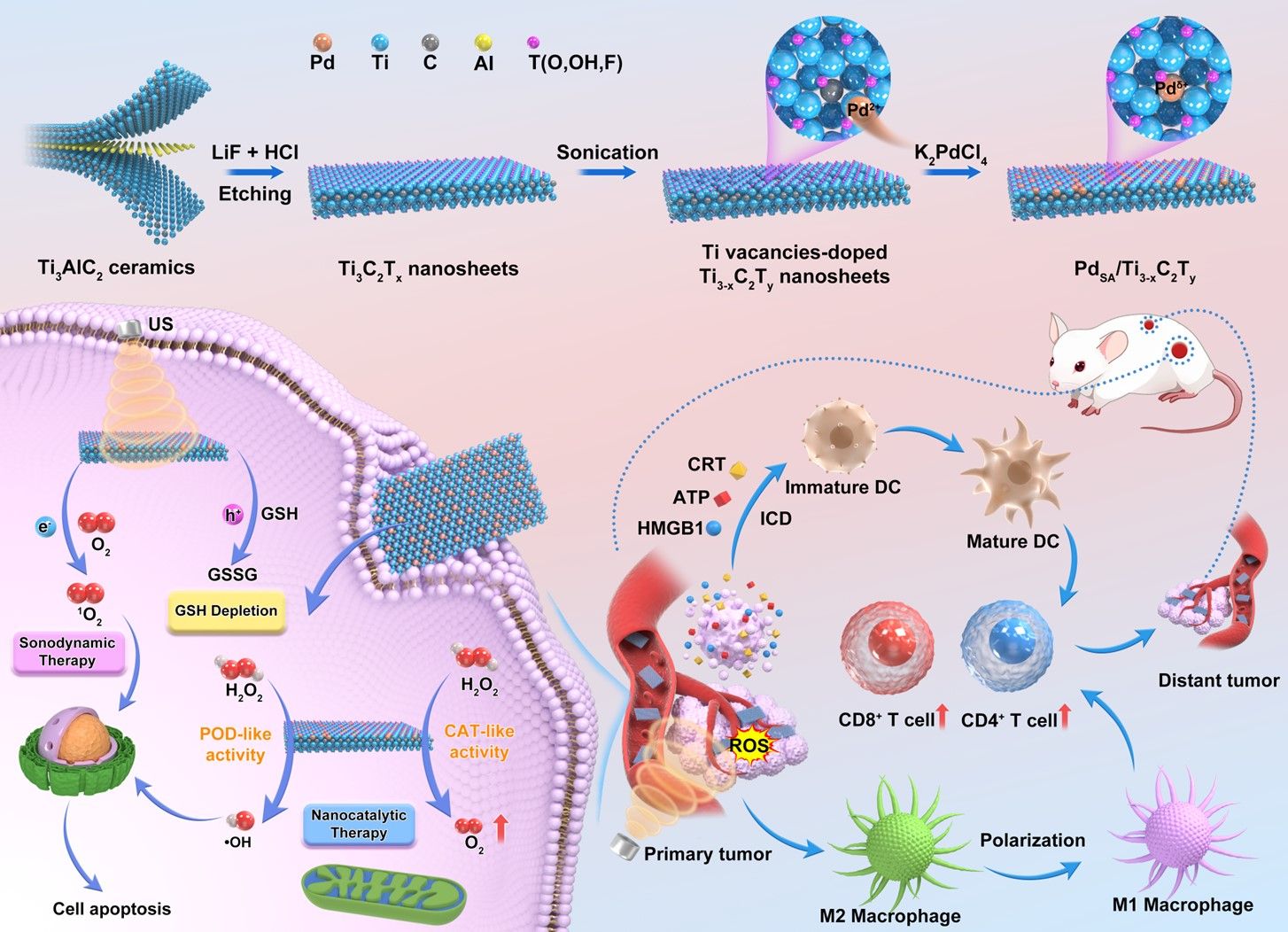
该团队创新性提出理性构筑单原子催化剂重塑肿瘤微环境的新策略,利用Ti3-xC2Ty纳米片中还原性Ti空位来稳定单原子Pd,获得的单原子催化剂中Pd的负载量高达2.5 wt%。与负载Pd纳米颗粒的Ti3-xC2Ty纳米片相比,单原子催化剂具有增强的声动力性能和纳米酶活性,这一现象归因于四个方面的协同作用。首先,单原子Pd的负载有效防止激发的电子空穴对再复合,显著提升声动力活性;其次,超声辐照下产生的空穴可以快速消耗肿瘤微环境中过表达的谷胱甘肽,进一步提升活性氧的产率;第三,单原子增强的类过氧化物酶活性可以催化产生•OH以实现对ROS产率的级联放大;最后,单原子增强的类过氧化氢酶活性可以缓解乏氧的肿瘤微环境,提供更多的O2供SDT产生ROS。更重要的是,SDT/CDT增强的免疫反应可以通过引发免疫原性死亡促进树突细胞成熟,同时可以将促肿瘤M2表型的肿瘤相关巨噬细胞极化为抗肿瘤的M1表型,最终实现对T细胞的激活。体内双侧肿瘤模型证明了单原子催化剂可以通过声动力免疫治疗将原发肿瘤完全消除,并可以通过强大的免疫反应减缓远端肿瘤的生长。该工作展现了单原子催化剂通过重塑肿瘤微环境实现强大的声动力免疫治疗的潜力。
该论文第一作者和通讯作者为我院青年教师耿弼江,共同第一作者为在站博士后胡金燕,共同通讯作者为我院潘登余教授和上海交通大学医学院附属第六人民医院沈龙祥教授,该研究得到了国家自然科学基金、中国科协青年人才托举工程、国家资助博士后研究人员计划和上海市自然科学基金等项目的资助。
耿弼江博士近年来聚焦于碳基纳米材料的微结构调控及其功能调控研究,在碳基量子点的生物医学应用领域积累了较丰富的研究成果和研究经验。近五年以第一或通讯作者在Nature Communications、Advanced Materials、Advanced Science、Small、Small Structures、Chemical Engineering Journal等国际期刊上发表SCI论文35篇,其中,发表在Nature Communications的论文入选了ESI高被引论文和ESI热点论文,该成果入选上海大学十大学术进展。近三年先后获得了多项人才计划和科研项目,2023年入选第九届中国科协青年人才托举工程,2020年入选上海市“超级博士后”激励资助计划,主持国家自然科学基金青年基金和中国博士后科学基金面上资助等科研项目。
论文链接:https://onlinelibrary.wiley.com/doi/10.1002/adma.202313670
