近日,我院耿弼江副研究员在Nature子刊《Nature Communications》上发表题为“D-π-A sensitized carbon dots as long-lived type-I/II photosensitizers for NIR-excited hypoxia-regulated photodynamic therapy”的研究论文。
光动力治疗(PDT)凭借其非侵入性、时空可控和免疫激活等优势,在肿瘤治疗领域展现出巨大潜力。然而,传统光敏剂普遍面临激发波长短、三重态寿命短、依赖氧气产生单线态氧等瓶颈,导致其在乏氧肿瘤微环境中的疗效严重受限。此外,如何实现单一近红外激光激发下的I/II型双模式PDT与温和光热治疗(PTT)的协同,同时避免对正常组织的热损伤,是当前PDT领域亟待解决的关键科学问题。
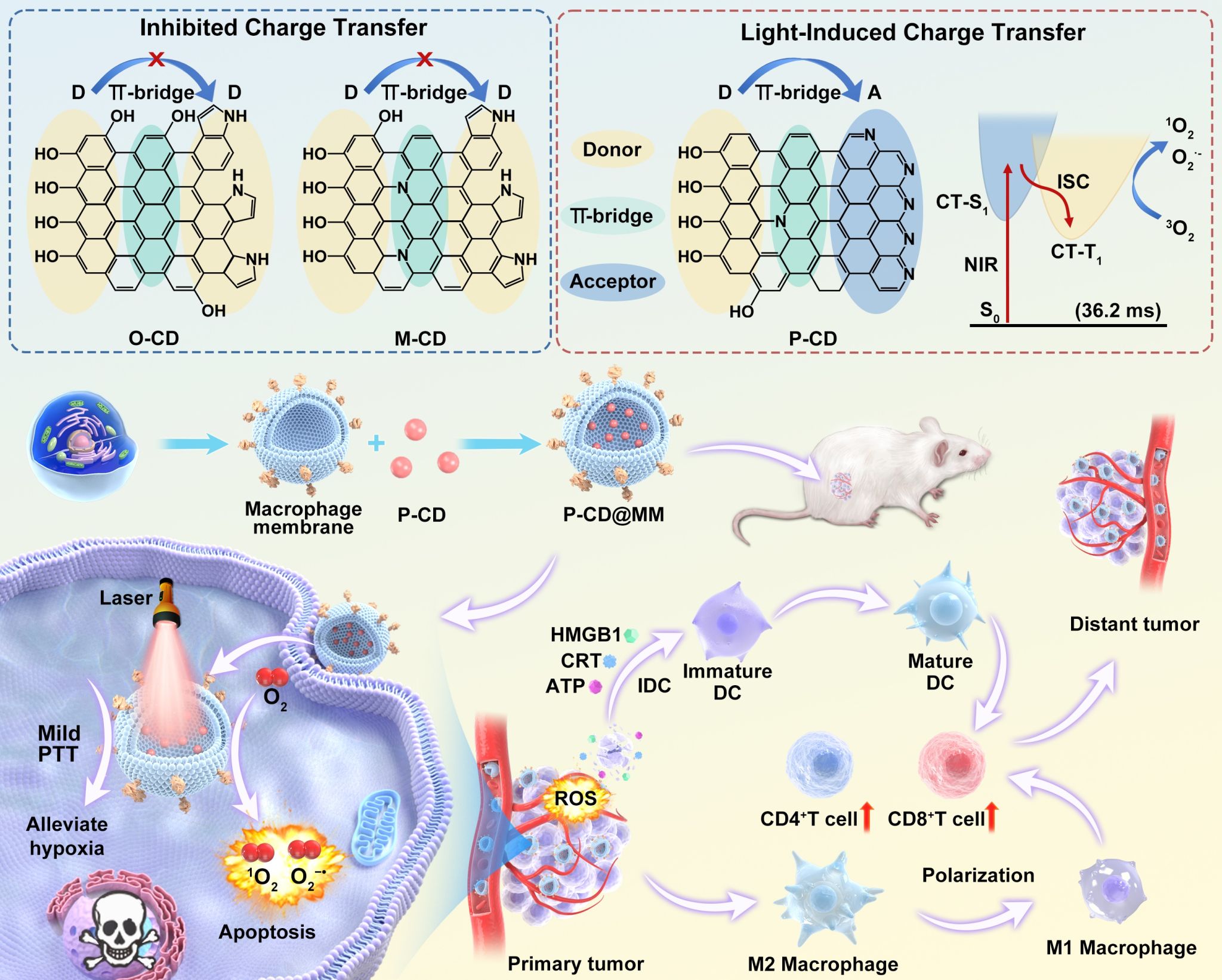
针对上述挑战,潘登余/耿弼江研究团队发展了一种二元前体工程策略,通过精准调控碳点的给体-π-受体(D-π-A)构型,以酚羟基为富电子给体、吡啶氮为吸电子受体,构筑了具有超长三重态寿命(36.2 ms)的近红外响应型I/II双模式光敏剂(P-CDs)。理论计算与实验结果表明,D-π-A结构诱导的分子内电荷转移态极大促进了系间窜越,缩小了单重态-三重态能隙,从而实现了高效的单线态氧(1O2)和超氧阴离子自由基(O2•ˉ)生成。与此同时,P-CDs表现出温和的光热转换效率(32.2%),可在低功率密度(0.30 W/cm2,808 nm)下实现温和的光热治疗,有效缓解肿瘤乏氧,进一步增强PDT疗效。研究团队进一步采用M1型巨噬细胞膜封装P-CDs(P-CD@MM),实现了主动靶向肿瘤富集与快速系统性清除。在双侧荷瘤小鼠模型中,经过静脉注射联合单次近红外激光照射,有效抑制了原发肿瘤的生长,还通过诱导免疫原性死亡、促进树突细胞成熟、将肿瘤相关巨噬细胞从促肿瘤的M2表型重极化为抗肿瘤的M1表型,显著抑制了远端肿瘤的生长,并建立了长期免疫记忆效应。
环化学院24级博士研究生张镇林为本文第一作者,耿弼江副研究员、潘登余研究员、上海交通大学医学院附属第六人民医院沈龙祥教授,同济大学附属第十人民医院史升副教授为共同通讯作者。上海大学为第一完成单位和通讯单位。该研究得到了国家自然科学基金、上海市自然科学基金、中国科协青年人才托举工程等项目的资助。
论文链接:https://doi.org/10.1038/s41467-026-71476-y
